Nuevos aspectos del cáncer de mamaPersonales
Ana Luisa Villanueva
Directora Médica de Vida, Salud & Accidentes
MAPFRE RE
Madrid - España



El cuerpo está formado por muchos tipos de células. Estas crecen y se multiplican de forma ordenada para mantener las funciones vitales, y el normal funcionamiento del cuerpo. En ocasiones, este proceso ordenado se descontrola. El material genético, o ADN, de la célula se altera produciendo mutaciones o cambios que afectan al crecimiento y funcionamiento celular. Cuando esto ocurre, se generan células que no mueren cuando deben morir, y forman nuevas células y estructuras que atraen vasos sanguíneos para nutrirse, constituyendo un tumor o cáncer.
El cáncer de mama es una de las patologías más relevantes que se presenta en la población de los países occidentales. En las mujeres es el tumor maligno más frecuente, y la primera causa de muerte, aunque su incidencia varía según el área geográfica. Las diferencias se atribuyen a los diversos hábitos de vida, los factores ambientales y los procedimientos diagnósticos utilizados. La incidencia de este tipo de cáncer aumenta con el nivel económico; se diagnostican más de la mitad de los casos mundiales en los países desarrollados.
Según la Agencia Internacional de Investigación del Cáncer (IARC, por sus siglas en inglés), la incidencia de esta enfermedad es más elevada a partir de los cuarenta años, aumentando de los cincuenta en adelante. Aunque la tasa de mortalidad ajustada es de 18,5 por ciento, se ha observado una clara tendencia a la disminución. En los hombres su presencia es poco frecuente; representan el uno por ciento de todos los tumores de mama. Es habitual que en estos casos se produzca un retraso en el diagnóstico, ya que no se tiene en cuenta esta posibilidad y su evolución es más rápida que en la mujer debido al menor volumen de la glándula mamaria.
Gracias a los programas de cribado, o screening, en la población, la tasa de incidencia ha aumentado y los avances en el diagnóstico y tratamiento han conseguido situar la supervivencia de mujeres en España por encima del 80 por ciento, según el estudio EUROCARE-4.
Aspectos biológicos de la enfermedad
Los aspectos biológicos definen los procesos y transformaciones característicos de estas células tumorales. Es importante conocerlos para entender el desarrollo de la enfermedad y los métodos diagnósticos que se utilizan.
Los tumores mamarios muestran frecuentemente una heterogeneidad que se manifiesta en aspectos fenotípicos:
- Morfología celular.
- Expresión génica.
- Marcadores de superficie.
- Factores de crecimiento.
- Receptores hormonales.
- Metabolismo.
- Angiogénesis.
- Motilidad.
- Proliferación.
- Inmunogenicidad.
- Potencial metastásico.
- La reprogramación metabólica
Las células tumorales se caracterizan por mostrar un metabolismo de la glucosa diferente al de la mayoría de los tejidos, debido a múltiples factores celulares y ambientales. Esto se traduce en una ineficiencia energética y un mayor flujo de glucosa. Esta característica se utiliza en el diagnostico radiológico con la Tomografía por Emisión de Positrones (PET, por sus siglas en inglés Positron Emission Tomography). Esta alteración determina un estímulo del crecimiento celular, la evasión de la apoptosis, o muerte celular, un potencial replicativo ilimitado, un aumento de la vascularización o formación de vasos, la invasión tumoral, las metástasis y el escape del sistema inmune. - La hipoxia, o falta de oxígeno
Esta característica se relaciona directamente con la agresividad, progresión y resistencia a ciertos fármacos quimioterápicos, además de inducir la expresión de numerosos genes a través de factores de transcripción. - Angiogénesis
Proceso fisiológico que consiste en la formación de vasos sanguíneos nuevos a partir de otros preexistentes. Si bien esta situación existe en condiciones normales como la cicatrización, es un fenómeno fundamental para que un tumor se desarrolle y crezca, no solo en su lugar de origen, sino también en las metástasis.
Los tumores estimulan la angiogénesis mediante la secreción de ciertos factores que inducen el crecimiento del endotelio vascular. - Senescencia - actividad telomerasa
La senescencia celular se define como la capacidad limitada de las células para poder dividirse más de un número determinado de veces. Cuando las células escapan a este proceso, se hacen inmortales. Este hecho está relacionado con los telómeros cromosómicos o estructuras especializadas situadas en los extremos de los cromosomas, que se acortan con cada división celular, de modo que -llegado un límite- no pueden dividirse más. - Presencia de macrófagos asociados
Hasta hace poco tiempo, la presencia de macrófagos en los tumores era considerada como una respuesta del huésped al tumor. Ahora se sabe que juegan un importante papel en la progresión e invasión del tumor, ya que su función es fagocitar los cuerpos extraños que penetran en el organismo.
Entre las funciones de los macrófagos asociados a tumores está la liberación de sustancias favorecedoras, factores estimulantes y activadores que favorecen la formación de vasos, el crecimiento, migración e invasión tumoral, la supresión inmune y la protección frente al tratamiento. - Células Stem
Estas células suponen menos del 0,1 por ciento de las células tumorales y se caracterizan por su auto renovación y por la producción de células progenitoras que pueden diferenciarse en células maduras y diferenciadas.
Estas células son más resistentes a la acción de los fármacos, incluyendo los quimioterápicos; y a la radioterapia. En la actualidad se utilizan como dianas terapéuticas. - Potencial metastásico - Metástasis óseas
En un 83 por ciento de las pacientes afectadas de tumores mamarios aparecen metástasis óseas, generalmente osteolíticas (destrucción de tejido óseo), aunque en un 15-20 por ciento son osteoblásticas (producción de tejido óseo). La afectación del hueso se produce por interacción del tumor con el entorno a través de la liberación de sustancias que facilitan la migración celular, la adhesión de las células tumorales a la matriz ósea, la liberación de factores que regulan la creación y formación de huesos y la supervivencia y proliferación de las células tumorales en el hueso.
Clasificación
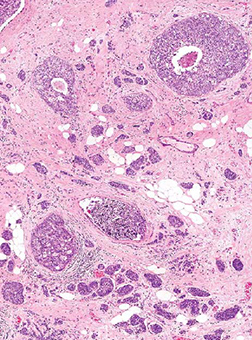
La valoración histológica de los carcinomas de mama sigue siendo la fuente principal de información pronóstica y predictiva más poderosa y el factor de discriminación principal para el diseño de terapias adyuvantes específicas.
El tipo histológico de tumor, tamaño, número de ganglios afectados y la existencia de metástasis, son los factores fundamentales para determinar el estadiaje del tumor.
Actualmente, el tratamiento personalizado del cáncer de mama se basa principalmente en la suma de las características histopatológicas (tamaño del tumor, tipo y grado, ganglios linfáticos afectados y metástasis) con factores biológicos como la sensibilidad a las terapias endocrinas, reflejados en parámetros biológicos como la expresión de receptores hormonales, para estrógenos (RE), para progesterona (RPg) y el estado del HER2 (Human Epidermal Growth Factor Receptor 2), o receptor 2 del factor de crecimiento epidérmico, que es un importante marcador y diana de tratamiento oncogénico, especialmente del cáncer de mama.
| Estadio | TNM |
|---|---|
| 0 | T0N0M0 |
| I | T1N0M0 |
| A | T0, T1N1M0 T2N0M0 |
| IIB | T2N1M0 T3N0M0 |
| IIIA | T0, T1, T2, N2 M0 T3N1 N2M0 |
| IIIB | T4 Cualquier N M0 |
| IIIC | Cualquier TN3M0 |
| IV | Cualquier T Cualquier N M1 |
Nueva clasificación - clasificación molecular
En los últimos años se han aplicado sofisticadas técnicas de análisis genético para estudiar las células tumorales de mama.
La relevancia clínica de la clasificación molecular radica fundamentalmente en mejorar los resultados terapéuticos, bien ahorrando a los pacientes con buen pronóstico los efectos secundarios de un tratamiento innecesario; o bien seleccionando realmente un subgrupo de pacientes con alta probabilidad de responder a un tratamiento específico.
Pruebas diagnósticas y de cribado
Según la OMS (Organización Mundial de la Salud), el cribado consiste en determinar la presunta existencia de una enfermedad o defecto no diagnosticados por medio de pruebas, exploración física u otros procedimientos que puedan aplicarse con rapidez. En el cáncer de mama estas pruebas son de vital importancia para la detección precoz, diagnóstico y tratamiento de la enfermedad. Veamos cuáles son.
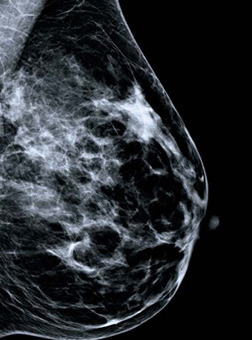
La mamografía
La mamografía es la prueba por excelencia en el diagnóstico del cáncer de mama.
Antes de efectuar un estudio mamográfico es preciso analizar la historia médica y los aspectos clínicos de la paciente, intentando buscar en la mamografía aquello que refiere la paciente y por lo que se consulta. Es decir, se debe adecuar el método radiológico a los datos médicos y clínicos recogidos. La correcta interpretación mamográfica requiere un especialista entrenado, capaz de correlacionar la información radiológica con la aportada por el paciente.
Es el método más extendido y el más fiable ya que muestra una sensibilidad próxima al 80 por ciento, que varía en función de múltiples factores: el tipo de estructura mamaria, el tipo de lesión, su morfología, ubicación, volumen mamario y la propia calidad radiológica de la imagen obtenida.
Entre un 10 y 15 por ciento de los cánceres con análisis histológico (del tejido) no tienen representación radiológica. Esta circunstancia obliga a disponer de una técnica de diagnóstico por imagen muy actualizada y, si es posible, completar el estudio con una ecografía para aumentar la sensibilidad.
La mamografía ha alcanzado en los últimos tiempos un gran desarrollo tecnológico y como consecuencia ha permitido avanzar en el diagnóstico. Los nuevos equipos digitales y las técnicas de manipulación de imagen nos están permitiendo aprender que el verdadero caballo de batalla es el cáncer subclínico, cuyo diagnóstico y tratamiento temprano aseguran una mayor supervivencia y aspecto plástico.
Signos radiológicos del cáncer de mama
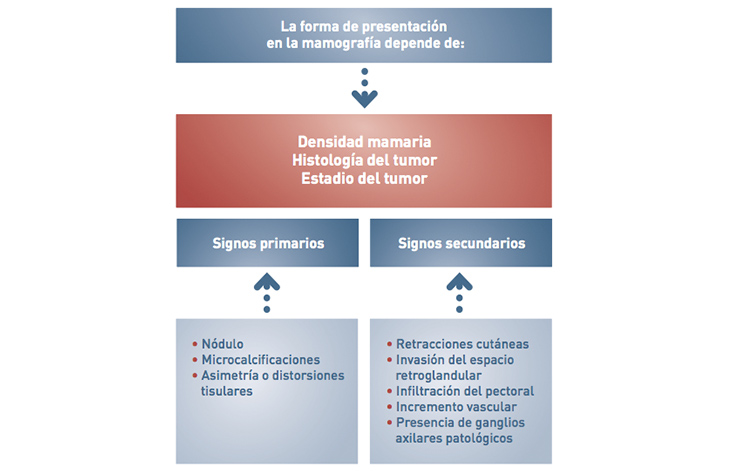
Nuevas técnicas de diagnóstico por imagen
La mamografía digital, o mamografía digitalizada
Es un sistema que elimina la necesidad de película, aprovechando la tecnología digital, tanto en imagen de pantalla, redes e impresión de la película como el archivo de las imágenes. Esta técnica optimiza la imagen y ofrece uniformidad en el espesor glandular mamario, ya que consigue una mejor visualización de los tejidos subcutáneos. Permite manipular la imagen, ampliarla, invertirla, realzarla o variar el brillo y el contraste, almacenarla en un CD o en un archivo electrónico; incluso puede imprimirse en una impresora láser de alta definición. Como no es necesario repetir proyecciones, evita la radiación derivada de estas.
No hay que olvidar que una mamografía convencional realizada en óptimas condiciones puede aportar información diagnóstica de muy alto nivel, aunque su registro se realice en una placa y la imagen no pueda manipularse.
Esta técnica digital es especialmente útil en las microcalcificaciones. Estas suelen ser el diagnóstico radiológico más frecuente del carcinoma in situ, con un gran valor en la detección precoz. Permite ver con claridad la forma y distribución de los depósitos, parámetros que determinan con mayor exactitud la sospecha de malignidad.
La Tomosíntesis Digital Mamaria (TDM)
Esta revolucionaria técnica en tres dimensiones permite realizar proyecciones individuales de múltiples cortes que, posteriormente, reconstruye en los diferentes ejes espaciales, obteniendo imágenes de alta resolución. Esto supone una mejor interpretación de las lesiones al evitar la superposición de imágenes. Es especialmente útil para lesiones nodulares y zonas de desestructuración.
La ecografía
Esta técnica ha pasado en muy pocos años de utilizarse tan sólo para diferenciar imágenes sólidas y quísticas, a ser un complemento imprescindible para establecer el grado de sospecha ante una lesión mamaria que en radiografía resulta indeterminada. Entre sus ventajas podemos incluir la capacidad para valorar la estructura interna de las lesiones en múltiples planos, su orientación, morfología y márgenes, tanto en mamas de predominio graso como en aquellas con estructura glandular densa, donde la mamografía es más limitada.
- Como técnica inicial está indicada en mujeres jóvenes, por debajo de los treinta años con mamas densas sintomáticas, así como en mujeres lactantes o embarazadas.
- Como técnica complementaria a la mamografía, tiene un papel fundamental: mamas portadoras de prótesis, estudio del árbol galactofórico en pacientes con secreciones, en mamografía negativa y lesión palpable, en mujeres con factores de riesgo y mamas densas y en casos de malignidad confirmada aportando datos como tamaño tumoral, afectación de piel y pectoral, multifocalidad y multicentricidad.
- También se usa como guía de procedimientos intervencionistas y marcaje prequirúrgico.
La ecografía 3D-4D
La aplicación de un programa informático específico a la técnica ultrasónica permite ver lesiones tumorales en un volumen tridimensional para estudiar la morfología de la lesión y su entorno. Este sofisticado programa permite realizar proyecciones en varios planos del espacio permitiendo valorar en volumen la forma e infiltración de procesos tumorales, así como la extensión a planos profundos y superficiales. También permite ver la posición de la aguja de biopsia para evidenciar la correcta posición con respecto a la lesión.
La elastosonografía
Esta técnica reciente se basa en el principio de la palpación mamaria, y permite hacer una estimación de la consistencia o la dureza de los tejidos. En el momento actual existen dos tipos:
La elastografía de compresión, o strain imaging, que valora la deformación de los tejidos y la elastografía supersónica, o supersonic shearwaves imaging, que permite conocer parámetros como la elasticidad máxima, mínima o media de las estructuras estudiadas.
Esta técnica debe ser entendida como un valor añadido a la ecografía y permite confirmar la hipótesis ecográfica de benignidad, reduciendo el número de biopsias innecesarias y orientar a pacientes de bajo riesgo hacia un seguimiento más seguro.
El PET-TC
El PET, conocido por sus siglas en inglés Positron Emission Tomography, o Tomografía por Emisión de Positrones, permite medir los procesos metabólicos localizados, y descubre las alteraciones metabólicas que anticipan a las anomalías anatómicas. Por su parte, el TC, TAC, o Tomografía Computarizada o Tomografía Axial Computarizada, también conocido como escáner, permite la obtención de múltiples imágenes a través de cortes o secciones anatómicas. La técnica híbrida PET-TAC muestra la actividad metabólica anormal, aportando información cualitativa y cuantitativa, de utilidad para el diagnóstico, tratamiento y pronóstico. En el cáncer de mama, la resolución espacial está limitada ya que no detecta lesiones con un diámetro inferior a diez milímetros.
El PEM
El PEM o Positron Emission Mamography surge de la limitación de la técnica arriba mencionada. Aunque en este momento se encuentra en fase de estudio clínico, ya arroja resultados superiores a la resonancia magnética.
Esta técnica tendrá su aplicación en la planificación quirúrgica, monitorización de la respuesta a tratamiento neo adyuvante, y monitorización de recurrencia. Los principales inconvenientes son el coste y la dificultad técnica del manejo del radiofármaco.
La imagen molecular
La imagen molecular es definida por la Sociedad Americana de Medicina Nuclear como la visualización, caracterización y medida de procesos biológicos en el ámbito molecular y celular en humanos y otros seres vivos. Esta técnica permite un seguimiento en tiempo real, no conlleva destrucción tisular y puede utilizarse en todos los estadios del tumor desde el cribado hasta las etapas más avanzadas. Se asocia a todas las técnicas radiológicas, simples y avanzadas, como la tomografía computarizada, la resonancia magnética, el ultrasonido o ecografía y PET, además de la imagen electromagnética no ionizante.
Cómo se trata el cáncer de mama
Los avances en el conocimiento de los mecanismos de diseminación de la enfermedad y la puesta en marcha de los programas de cribado poblacional, han dado como resultado el diagnóstico de la enfermedad en etapas cada vez más tempranas y una importante evolución en su tratamiento.
La cirugía oncoplástica
La cirugía oncoplástica aporta soluciones quirúrgicas que permiten la reconstrucción estética de la mama tras una mastectomía o durante una cirugía conservadora, así como la corrección de secuelas de otros tratamientos. Incluye diversas técnicas de mamoplastia, estrumoplastia, reconstrucción mamaria y cirugía de reducción de riesgo.
La reconstrucción mamaria suele necesitar más de una intervención para obtener el resultado estético adecuado. Puede estar indicada tanto como cirugía profiláctica, en casos de alto riesgo, como en estadios iniciales o avanzados de la enfermedad, lo que condicionará la reconstrucción en el mismo acto quirúrgico o de forma diferida.
El tratamiento hormonal
Gracias a los estudios para determinar los receptores hormonales sabemos que aquellas pacientes que son positivas tanto para estrógenos como para progesterona responden en más del 50 por ciento de los casos. Cuanto mayor es el número de células que los tienen, y mas alta su concentración, mayores son las posibilidades de respuesta. Dependiendo de los casos, ayuda a disminuir la aparición de tumor en la mama contralateral.
La quimioterapia
La quimioterapia junto con la terapia diana y la hormonoterapia representan el abordaje sistémico actual del cáncer de mama. El éxito del tratamiento radica en la reducción o ideal eliminación definitiva de la posibilidad de recidiva, cuya probabilidad es directamente proporcional a la eficacia de la terapia e inversamente proporcional al riesgo de recidiva inherente al tumor, medida a través de los factores pronósticos.
Elementos de la toma de decisión terapéutica
Se entienden por factores pronósticos aquellos que aportan información del resultado clínico en el momento del diagnóstico, independientemente de la terapia que se vaya a aplicar.
Los factores pronósticos de riesgo requieren una serie de características para ser aceptados como tales. Su uso debe ser sencillo, de bajo consumo de recursos, reproducible, fácilmente disponible e interpretable por el clínico. Los únicos marcadores disponibles que cumplen con estas condiciones son: la clasificación TNM, el grado histológico, el estado menopáusico, la expresión de RH, el tipo histológico y la edad.
Actualmente son factores pronósticos reconocidos:
- Clasificación TNM.
- Fenotipo tumoral: grado tumoral, expresión RH, invasión linfovascular o expresión HER2.
- Edad < 35 años.
En la décima primera conferencia, en 2009, del International Breast Cancer Group (IBCG) se consideró más adecuada la toma de decisiones basada en factores que predicen la respuesta al tratamiento que en aquellos que pronostican el riesgo; eliminando, de este modo, las categorías de riesgos para dar paso a las recomendaciones terapéuticas, en función de la posibilidad de respuesta al tratamiento; los receptores hormonales, RH, y la expresión HER2 son los únicos predictores conocidos.
La radioterapia
Es aconsejable la elección de un centro que cuente con la tecnología adecuada y un equipo multidisciplinar para una decisión personalizada del tratamiento.
Desde hace más de treinta años, el tratamiento habitual estándar para pacientes con cáncer de mama, después de una cirugía conservadora, ha sido la radioterapia externa que implica la irradiación diaria en el transcurso de seis semanas.
En los últimos diez años se han venido desarrollando dos nuevas. Una en relación a la duración del tratamiento, lo que implica menos fracciones con aumento de dosis. La otra en relación a la cantidad de tejido mamario sometido a radiación ionizante.
De aquí surgen dos nuevos acercamientos:
- La Radiación Parcial de la Mama, o PBI (Partial Breast Irradiation)
La PBI limita el volumen del tratamiento al lecho tumoral y tejido mamario adyacente, generalmente con un margen de uno a dos centímetros, sin incluir todo el volumen mamario. - La Radioterapia Intraoperatoria, o IORT (Intra Operative Radiation Therapy)
Esta consiste en irradiar, con una sola dosis externa, los diferentes tipos de tumores.
Desde comienzos de este siglo se ha empezado a utilizar una técnica combinada de los planteamientos anteriores: la Radioterapia Intraoperatoria con Electrones, o ELIOT (Electron Intraoperative Therapy), que suministra una sola dosis de radiación equivalente a la dosis total con radioterapia externa fraccionada, después de la resección amplia o cuadrantectomía, utilizando un acelerador lineal móvil situado en quirófano. Con esta técnica es posible tratar solo el cuadrante afectado de la mama, acortando el curso de radioterapia de seis semanas a una sola sesión de tres minutos durante la cirugía.
Perspectiva para el mundo asegurador
Los continuos avances científicos, tanto diagnósticos como terapéuticos, suponen no solo un aumento en las expectativas de vida sino una mejora en la calidad de vida. Para el mundo asegurador esto implica una adecuación y puesta al día constante, no solo en el diseño de nuevos productos sino en la incorporación de todas estas tecnologías a los servicios que se ofrecen dentro de los mismos.
La inclusión en los seguros médicos de nuevas técnicas de cribado, análisis para la detección de factores pronósticos y pruebas genéticas para la determinación de mutaciones génicas, todos ellos muy necesarios para el adecuado tratamiento, significan una elevación de los costes y una mejora de la calidad de los servicios ofertados. Esto conlleva un mejor posicionamiento en el proceso de toma de decisión por parte del potencial asegurado, un cambio positivo en la percepción del consumidor y un aumento de la prima, en algunos casos.
El tiempo de crisis en que nos encontramos no favorece el planteamiento de inversión en equipamiento más sofisticado, pero sí está generando la aparición de nuevos productos con coberturas más específicas, como es el caso de la cobertura de enfermedades graves para cánceres específicos, o exploraciones de cribado asociadas a otros elementos de la medicina preventiva.
Para la selección de riesgos en los seguros personales, estos avances suponen un replanteamiento en los cuestionarios médicos y las pruebas médicas que se soliciten. El diagnóstico precoz, junto con el tratamiento de enfermedades avanzadas, están permitiendo una estratificación mejor del riesgo, lo que conduce a la aceptación de un mayor número de casos, con una prima más ajustada, a la situación real del candidato.
La aportación de una información más precisa en la valoración del siniestro permitirá acelerar el proceso de decisión y actualizar la selección de riesgos para facilitar dicha toma de decisión.
La incorporación de estas novedades científicas ha supuesto también un cambio en la legislación. La capacidad predictiva de muchos de los nuevos tests ha hecho que los organismos reguladores se ocupen de acotar el uso de la información que se desprenda de ellas, preservar el derecho a la intimidad de la persona y evitar la discriminación.
Los seguros personales tienen el reto de asimilar estas novedades para mejorar los productos y servicios y redefinir los niveles de riesgo.
Quiero expresar mi agradecimiento al Centro de Patología de la Mama Dr. Tejerina por haberme proporcionado la información necesaria para la realización de este artículo. La Autora.



